COVID-19
Choroba zakaźna wywoływana przez SARS-CoV-2 (Severe Acute Respiratory Syndrome Coronavirus 2), ß-koronawirusa z rodziny Coronaviridae. Rezerwuarem patogenów, podobnie jak w przypadku innych, wysoce patogennych koronawirusów (SARS-CoV-1, MERS-CoV) są zwierzęta (prawdopodobnie nietoperze; potencjalnym nosicielem pośrednim są łuskowce i/lub cywety). Po przełamaniu bariery międzygatunkowej zakażenie przenosi się z człowieka na człowieka; źródłem zakażenia są zarówno chorzy, jak i zakażeni bez objawów chorobowych. Do zakażenia u ludzi dochodzi drogą kropelkową (inhalacja kropelek zakaźnej wydzieliny z dróg oddechowych osoby zakażonej) w wyniku bezpośredniego kontaktu z chorymi lub bezobjawowymi nosicielami (podczas kaszlu, kichania, rozmowy) oraz pośrednio przez kontakt z zakaźnymi wydzielinami i ich autoinokulacją do ust, nosa lub oczu (SARS-CoV-2 może utrzymywać się na różnych powierzchniach od kilku godzin do kilku dni). Osoby zakażone mogą być zakaźne dla otoczenia na 24-48 godzin przed wystąpieniem objawów, co w znaczący sposób ułatwia rozprzestrzenianie się zakażeń w populacji i utrudnia monitorowanie osób z kontaktu. Badania nad SARS-CoV-2 wykazały również obecność zakaźnych cząstek wirusa w kale i w moczu, co sugeruje możliwość jego replikacji w przewodzie pokarmowym i moczowym. Badania środowiskowe z kolei wykryły obecność wirusa w ściekach komunalnych, co może okazać się pomocnym narzędziem diagnostycznym do wykrywania krążenia SARS-CoV-2 w populacji.
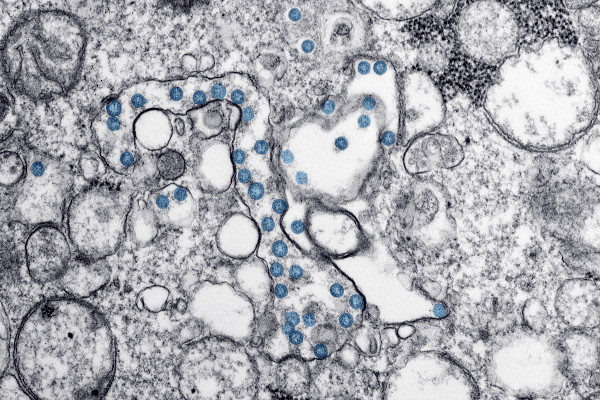
Źródło: CDC/Hannah A. Bullock, Azaibi Tamin
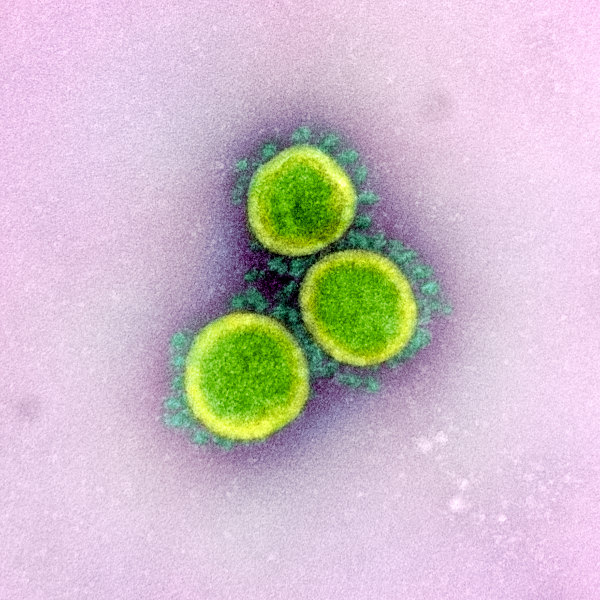
Źródło: National Institute of Allergy and Infectious Diseases (NIAID)
Epidemiologia
COVID-19 został rozpoznany w grudniu 2019 r. w środkowych Chinach (Wuhan, prowincja Hubei). W związku z rozprzestrzenianiem się choroby na kolejne kraje, 30.01.2020 r. WHO ogłosiła stan zagrożenia dla zdrowia publicznego o zasięgu międzynarodowym. Dynamiczny wzrost liczby zakażeń i zgonów na świecie (współczynnik śmiertelności CFR szacowany w tamtym okresie na 3-4%) spowodował ogłoszenie przez WHO 11.03.2020 r. stanu pandemii. Po ponad roku od ogłoszenia pandemii na świecie (stan na dzień 10.04.2021 r.), w 192 krajach i regionach na 6 kontynentach wykryto łącznie ponad 135 mln zakażeń i ponad 2,9 mln zgonów, najwięcej w Stanach Zjednoczonych (>32 mln zakażeń/>574 tys. zgonów), Brazylii (>13,4 mln/>349 tys.) i Indiach (>13,3 mln/>169 tys.). W Polsce w okresie 03.2020-04.2021 wykryto łącznie >2,6 mln zakażeń oraz >60 tys. zgonów. Na przebieg epidemii w poszczególnych krajach mają wpływ takie czynniki jak: stan opieki zdrowotnej (zabezpieczenie placówek medycznych w personel i sprzęt); zakres nałożonych restrykcji i ich przestrzeganie przez mieszkańców; stan zdrowotny społeczeństwa, ze szczególnym uwzględnieniem odsetka chorób przewlekłych (nowotwory, cukrzyca, otyłość, choroby układu krążenia, układu oddechowego, choroby nerek, niedobory odporności); struktura demograficzna społeczeństwa (odsetek osób w podeszłym wieku). Kluczowym wskaźnikiem do monitorowania dynamiki rozwoju epidemii jest współczynnik reprodukcji Ro (określający liczbę nowych zakażeń pochodzących od jednego zakażonego; wartość >1 oznacza, że epidemia się rozwija, tzn. jedna osoba zakażona przenosi zakażenie na >1 osobę) oraz współczynnik śmiertelności IFR (infection fatality rate, liczba zgonów z powodu COVID-19 w jednostce czasu w stosunku do liczby zakażonych). Ze względu na powszechne występowanie bezobjawowych zakażeń (szacowane na 80% przypadków) i stosunkowo niską liczbę wykonywanych testów wykrywających zakażenia SARS-CoV-2 w większości krajów (w tym w Polsce), powszechnie stosowanym parametrem na świecie jest współczynnik śmiertelności CFR (case fatality rate, czyli liczba zgonów z powodu COVID-19 w jednostce czasu w stosunku do liczby wykrytych przypadków choroby). Reasumując, CFR w Polsce i na świecie wynosi >2%, IFR jest wielokrotnie niższy i stanowi ułamek procenta.
Obraz kliniczny
Okres wylęgania wynosi 2-14 dni, średnio 5-6 dni. Zdecydowana większość osób (przyjmuje się, że 80%) przechodzi zakażenie bezobjawowo (będąc jednak źródłem zakażenia dla otoczenia) lub ma łagodne objawy o charakterze choroby przeziębieniowej, 15% wymaga leczenia szpitalnego, najczęściej w związku ze stanami zapalnymi dolnych dróg oddechowych; u 5% pacjentów choroba przebiega ciężko, z niewydolnością oddechową wymagającą w wielu przypadkach wentylacji mechanicznej. Do najczęstszych objawów chorobowych podczas łagodnego przebiegu należą: gorączka, suchy kaszel, zaburzenia węchu i/lub smaku, odkrztuszanie plwociny, zmęczenie, bóle mięśni i stawów. W stanach średniociężkich pojawiają się kliniczne i radiologiczne objawy zapalenia dolnych dróg oddechowych z saturacją (wskaźnik nasycenia hemoglobiny krwi obwodowej tlenem) ≥94%. W stanach ciężkich saturacja spada <94%, częstość oddechów ≥30/min, zmiany naciekowe w płucach występują w ponad 50% przypadków. W stanie krytycznym występują objawy ostrej niewydolności oddechowej, wstrząsu septycznego, niewydolności wielonarządowej, w tym ostrej niewydolności krążenia, ostrego uszkodzenia nerek, zaburzeń czynności wątroby (u pacjentów, u których choroba zakończyła się zgonem, czas od wystąpienia objawów do śmierci wynosił średnio od 2 do 8 tygodni). Na obecnym etapie wiedzy przyjmuje się, że dzieci nie obciążone wywiadem chorobowym przechodzą COVID-19 łagodniej niż dorośli. Do grupy ryzyka ciężkiego przebiegu choroby należą osoby w podeszłym wieku, z niedoborami odporności, obciążone chorobami przewlekłymi (nowotwory, cukrzyca, otyłość, choroby układu sercowo-naczyniowego, przewlekła obturacyjna choroba płuc, choroby nerek).
Do najczęstszych powikłań po przebyciu COVID-19 (według obecnego stanu wiedzy) należy zwłóknienie płuc z przewlekłą niewydolnością oddechową, powikłania sercowo-naczyniowe (zapalenie mięśnia sercowego, zmiany zakrzepowo-zatorowe naczyń) neurologiczne (udar, zapalenie mózgu i rdzenia kręgowego) i psychiatryczne (stany lękowe, depresyjne, zaburzenia pamięci, koncentracji). Powikłania odległe w czasie mogą wystąpić również u osób, które przebyły zakażenie SARS-CoV-2 bez objawów COVID-19, co utrudnia ustalenie pierwotnej przyczyny zmian chorobowych (np. zmniejszonej tolerancji wysiłku lub duszności spoczynkowej).
Rozpoznanie
Podstawą rozpoznania zakażenia jest wykrycie wirusów metodami molekularnymi (RT-PCR, reakcja łańcuchowej polimerazy w czasie rzeczywistym); materiałem diagnostycznym jest wymaz z jamy nosowo-gardłowej (badanie materiału genetycznego wirusa znajdującego się w nabłonku dróg oddechowych). Metodami pomocniczymi o charakterze przesiewowym są metody immunoenzymatyczne (określanie miana przeciwciał; ok. 1–3 tygodni od zakażenia, ok. 10. dnia od czasu wystąpienia pierwszych objawów chorobowych) oraz immunochromatograficzne (testy antygenowe); materiałem diagnostycznym jest krew. W procesie diagnostycznym oprócz wykrycia czynnika etiologicznego, istotne są również dane z wywiadu epidemiologicznego, obraz kliniczny pacjenta oraz badania dodatkowe: tomografia komputerowa klatki piersiowej wykazuje zmiany zapalne w płucach (obwodowe zagęszczenia miąższu i zwłóknienia, objaw atolu -'odwróconego halo’, obraz ‘kostki brukowej’, mnogie zacienienia typu ‘matowej szyby’); w morfologii krwi występuje leukopenia, limfopenia, trombocytopenia, wzrost poziomu markerów zapalnych (CRP, OB, fibrynogen); w związku z częstymi powikłaniami pulmonologicznymi i kardiologicznymi zalecane jest wykonanie spirometrii płuc i EKG.
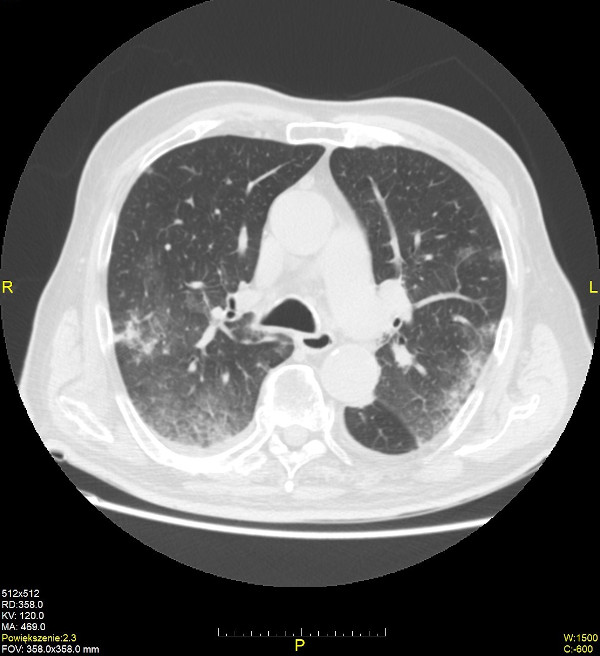
Źródło: Pracownia Rentgenodiagnostyki Szpitala im. św. Wincentego a Paulo w Gdyni
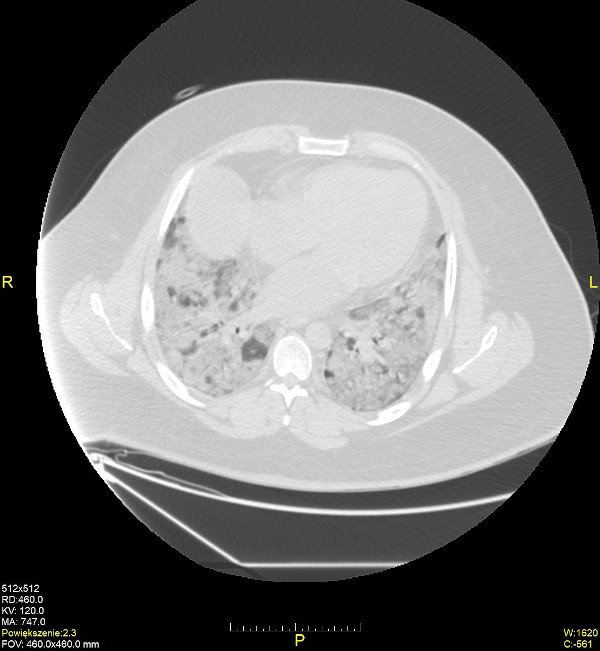
Źródło: Pracownia Rentgenodiagnostyki Szpitala im. św. Wincentego a Paulo w Gdyni
Leczenie
Na obecnym etapie wiedzy, nie ma zatwierdzonej, celowanej metody terapii COVID-19. Prowadzi się leczenie objawowe i podtrzymujące. Przypadki łagodne leczone są w trybie ambulatoryjnym podobnie, jak większość wirusowych infekcji układu oddechowego. W stanach średniociężkich i ciężkich, w warunkach szpitalnych stosuje się tlenoterapię i leczenie blokujące replikację wirusa SARS-CoV-2 (remdesivir; skuteczny u pacjentów z zapaleniem płuc i zagrażającą niewydolnością oddechową) oraz podaje osocze ozdrowieńców (sprawdzenie przed podaniem obecności przeciwciał neutralizujących SARS-CoV-2), które podobnie jak remdesivir jest skuteczne w fazie wiremii (namnażania się wirusa w organizmie chorego). Uzasadnione jest również stosowanie leczenia hamującego reakcję zapalną (deksametazon), znacząco zmniejszającego ryzyko zgonu (skutecznego przed wystąpieniem niewydolności oddechowej). W stanach krytycznych, w warunkach oddziału intensywnej terapii u osób z ostrą niewydolnością oddechową (ARDS) wprowadza się wentylację mechaniczną (respirator), której celem jest minimalizacja uszkodzenia pęcherzyków płucnych. Najczęściej stosowanym sposobem dostarczenia wdechu podczas wentylacji pacjentów z ARDS jest tryb objętościowy, który charakteryzuje się stałą objętością oddechową (w mililitrach) dostarczaną z każdym wdechem, niezależnie od mechanicznych właściwości płuc (ciśnienie generowane przez respirator w czasie kolejnych wdechów może się zmieniać). Postępowanie farmakologiczne w poszczególnych stadiach klinicznych zakażenia SARS-CoV-2 zalecane przez Polskie Towarzystwo Epidemiologów i Lekarzy Chorób Zakaźnych (PTEiLChZ) przedstawia tabela 3.8.
Tabela 3.8. Zalecane postępowanie farmakologiczne w poszczególnych stadiach klinicznych zakażenia SARS-CoV-2
| Stadium choroby | Leczenie podstawowe | Leczenie wspomagające |
|---|---|---|
stadium bezobjawowe lub skąpoobjawowe
|
|
|
| stadium pełnoobjawowe (namnażanie wirusa)
|
|
|
| stadium z niewydolnością oddechową (burza cytokinowa)
|
|
|
| stadium ostrej niewydolności oddechowej (ARDS)
|
|
|
Źródło: Flisiak R, et al. Zalecenia diagnostyki i terapii zakażeń SARS-CoV-2 Polskiego Towarzystwa Epidemiologów i Lekarzy Chorób Zakaźnych z dnia 13 października 2020 r. Aneks 2 do rekomendacji z 31 marca 2020 r. Medycyna Praktyczna 2020;11: 51-69.
Zapobieganie
Do podstawowych metod prewencji należą dystans społeczny (co najmniej 1,5-2 m, zwłaszcza od osób kaszlących, kichających, nie mających zakrytych ust i nosa), częste mycie i dezynfekcja dłoni (na bazie 70% alkoholu; SARS-CoV-2 jest wrażliwy na środki dezynfekcyjne) oraz noszenie masek ochronnych (zasada DDM – dystans społeczny, dezynfekcja, maski ochronne). Osoby z rozpoznanym zakażeniem SARS-CoV-2 podlegają izolacji (kończy się po 10 dniach u pacjenta bezobjawowego; może zostać przedłużona do 20 dni u pacjentów bezobjawowych o obniżonej odporności, obciążonych chorobami przewlekłymi; u pacjentów objawowych izolacja może zakończyć się po 3 dniach od ustąpienia gorączki i objawów infekcji dróg oddechowych, jednak nie wcześniej niż po 13 dniach od początku objawów chorobowych), natomiast osoby zdrowe mające styczność z osobą zakażoną oraz osoby przekraczające granice Polski i powracające do kraju – podlegają kwarantannie (w Polsce od 09.2020 r. okres kwarantanny wynosi 10 dni i ulega automatycznie zakończeniu, jeśli u danej osoby nie wystąpią objawy chorobowe; z kwarantanny zwalnia podróżnych negatywny wynik testu PCR lub antygenowego, jak również szczepienie przeciw COVID-19). Najskuteczniejszym środkiem zapobiegawczym są obecnie szczepienia ochronne różnych producentów oparte zasadniczo na dwóch różnych technologiach: szczepionki mRNA (Pfizer/BioNTech, Moderna, CureVac) oraz szczepionki wektorowe (producenci AstraZeneca, Johnson&Johnson). Szczepionki mRNA są produktami syntetycznymi (nie posiadającymi cząstek wirusa), zawierającymi fragment mRNA zsyntetyzowany metodami inżynierii genetycznej, który organizm człowieka poddanego szczepieniu traktuje jako matrycę do produkcji białka S koronawirusa i wytwarzania przeciw niemu swoistych przeciwciał. W szczepionkach wektorowych wykorzystuje się fragmenty innych wirusów (AstraZeneca zastosowała nieaktywną cząstkę adenowirusa wywołującego zmiany chorobowe u szympansów) do wywołania odpowiedzi immunologicznej przeciw wirusowi SARS-CoV-2. Bezwzględnym przeciwwskazaniem do szczepień jest alergia na którykolwiek ze składników produktów szczepionkowych. W przypadku szczepionek mRNA takim składnikiem może być glikol polietylenowy (PEG), natomiast w przypadku szczepionek wektorowych polisorbat 80. Obie substancje są wykorzystywane w produkcji leków i kosmetyków. Do innych przeciwwskazań (podobnie jak i przy podawaniu innych szczepionek) należą wysoka gorączka, inne objawy ostrej infekcji układu oddechowego, nieunormowany stan zdrowia pacjentów z chorobami przewlekłymi (cukrzyca, nadciśnienie tętnicze). Przy obecnym stanie wiedzy nie wiadomo, jaki poziom przeciwciał ochronnych jest wystarczający do ochrony przed zakażeniem SARS-CoV-2 oraz jak długo będzie utrzymywać się po szczepieniu (monitorowanie poszczepiennej odpowiedzi immunologicznej jest kluczowym elementem oceny skuteczności immunoprofilaktyki). Szacuje się, że odporność zbiorową w przypadku COVID-19 uzyska się, jeśli ponad 70% populacji będzie miała specyficzne przeciwciała ochronne (im większa zaraźliwość patogenu, tym większy odsetek populacji musi być uodporniony).
