Malaria
Jest chorobą pasożytniczą wywoływaną u ludzi przez pięć gatunków zarodźców: Plasmodium falciparum (zarodziec sierpowaty), Plasmodium vivax (zarodziec ruchliwy), Plasmodium malariae (zarodziec pasmowaty), Plasmodium ovale (zarodziec owalny) i Plasmodium knowlesi (zarodziec małpi). Transmisję i zarażenie P. knowlesi obserwuje się u zwierząt, przypadki zachorowań u ludzi rozpoznano w Azji Południowo-Wschodniej (gatunek tego zarodźca traktuje się jako formę odzwierzęcą). Do zachorowania na malarię u człowieka dochodzi w wyniku ukłucia przez zarażone zarodźcem komary (wprowadzające inwazyjne formy Plasmodium do krwiobiegu człowieka), przez przetoczenie krwi zawierającej trofozoity lub schizonty Plasmodium bądź drogą wertykalną z matki na płód. Zarodźce malarii są pierwotniakami pasożytującymi u człowieka w wątrobie oraz w krwinkach czerwonych krwi obwodowej.
Występowanie
W rejonach endemicznych malarii żyje 3,3 miliarda ludzi w 104 krajach. Według WHO, na zimnicę w 2017 r. chorowało 219 milionów osób (92% w Afryce, w tym 80% w 15 krajach: 25% w Nigerii, 11% w Demokratycznej Republice Konga, 5% w Mozambiku, 4% w Ugandzie; 5% w Azji Południowej i Południowo-Wschodniej, w tym 4% w Indiach). W tym samym czasie raportowano 435 tysięcy zgonów (93% w Afryce, 61% wśród dzieci poniżej 5. roku życia); 80% przypadków w 17 krajach, a 53% w 7 krajach: 19% w Nigerii, 11% w Demokratycznej Republice Konga, 6% w Burkina Faso, 5% w Tanzanii, 4% w Sierra Leone, 4% w Nigrze, 4% w Indiach. Najczęstszym czynnikiem etiologicznym zachorowań jest P. falciparum i P. vivax (80–95%). W krajach wysoko uprzemysłowionych (Ameryka Północna, Europa Zachodnia) rocznie odnotowuje się około 10 tysięcy zarażeń importowanych z rejonów występowania choroby, głównie z Afryki Subsaharyjskiej i Azji Południowo-Wschodniej. Sporadycznie notowane są również przypadki tzw. malarii lotniskowej lub portowej, czyli zachorowania w okolicach lotnisk i portów krajów, w których choroba nie występuje, a wektory zarażenia (komary) przedostają się do strefy klimatu umiarkowanego środkami transportu (samoloty, statki). W ostatnich latach przypadki rodzimej malarii w Europie raportowano w Grecji w 2013 r.; w 2016 r. pojedyncze zachorowania wśród Greków pojawiły się ponownie (transmisją choroby zagrożonych jest 12 gmin od Salonik po Peloponez). W Polsce corocznie diagnozuje się i leczy 20-30 pacjentów chorujących na malarię, którą importowali z rejonów endemicznego występowania choroby.
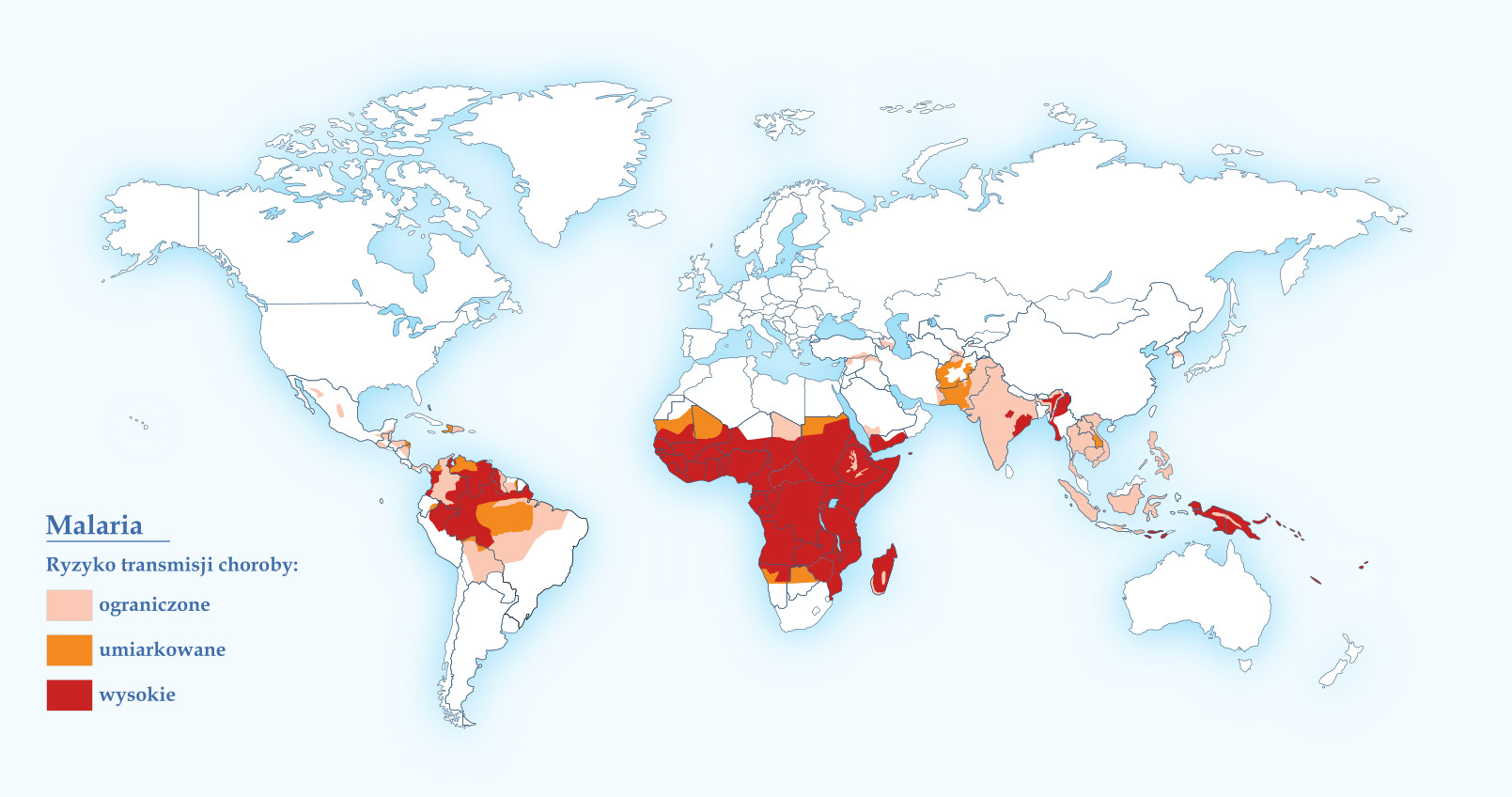
Sporadycznie spotykane są również przypadki tzw. malarii lotniskowej lub portowej, czyli zachorowania w okolicach lotnisk i portów krajów, w których choroba nie występuje, a wektory zarażenia (komary) przedostają się do strefy klimatu umiarkowanego środkami transportu (samoloty, statki).
Wektor zarażenia
Malaria przenoszona jest przez samice komarów widliszków z rodzaju Anopheles. Wektory zarażenia w rejonach malarycznych bytują zazwyczaj na wysokości do 2000 m n.p.m. (wyjątek stanowią niektóre rejony Afganistanu, Boliwii, Etiopii, Erytrei, Kenii i Pakistanu, gdzie notuje się przypadki transmisji choroby na wysokości 2200-2500 m n.p.m.).
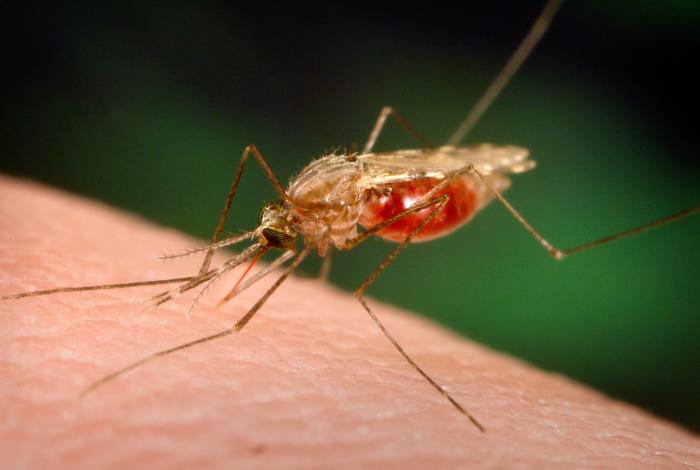
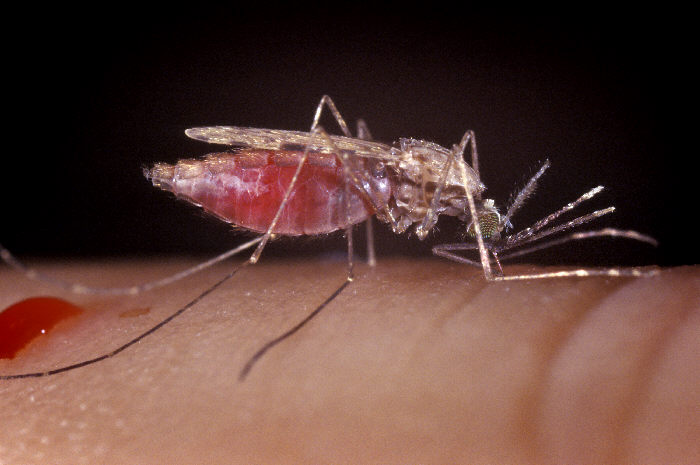
Cykl rozwojowy komara widliszka jest uzależniony od warunków klimatycznych: w temp. >30°C trwa 7 dni, a w temp. 20°C powyżej 3 tygodni. Poniżej 16°C dochodzi do zatrzymania cyklu rozwojowego pasożytów w wyniku odrętwienia komarów, spowodowanego zbyt niską temperaturą. Pasożyty jednak nie giną, a ich cykl rozwojowy jest tylko czasowo zatrzymany. Aby komary – wektory zarażenia – mogły się rozmnażać, potrzebują środowiska wodnego, w którym składane są jaja, następnie rozwijają się larwy, a z nich osobniki dorosłe.
Cykl rozwojowy Plasmodium
W organizmie samicy komara widliszka następuje sporogonia, czyli faza płciowa cyklu rozwojowego Plasmodium. Kąsając człowieka chorego na malarię komar poprzez aparat kłująco-ssący wprowadza do swojego organizmu wraz krwią zarażonego gametocyty męskie i żeńskie Plasmodium, które łącząc się tworzą zygotę. Zygota powiększając się zyskuje umiejętność poruszania (ookineta), aktywnie penetruje ścianę żołądka, gdzie ulegając encystacji tworzy oocystę. Wewnątrz oocyty dochodzi do licznych podziałów, w wyniku których powstają tysiące sporozoitów (formy inwazyjne dla człowieka), które migrują do gruczołów ślinowych komara, skąd przez aparat kłująco-ssący, wraz ze śliną podczas kolejnego ukąszenia, dostają się do układu krwionośnego człowieka. W ten sposób faza płciowa cyklu życiowego Plasmodium w organizmie komara ulega zakończeniu (w zależności od gatunku pasożyta i temperatury otoczenia trwa 8-35 dni), a rozpoczyna się schizogonia – faza bezpłciowa cyklu Plasmodium w organizmie człowieka. Inwazyjne sporozoity przez podskórne naczynia włosowate dostają się do krwiobiegu, gdzie utrzymują się przez około 0,5 godziny. Część z nich jest niszczona przez komórki układu odpornościowego człowieka, jednak większość dostaje się do hepatocytów, gdzie rozpoczyna się stadium schizogonii wątrobowej, trwającej w zależności od gatunku Plasmodium 6-16 dni (w tym czasie nie występują żadne objawy kliniczne choroby).
Sporozoity wnikają do hepatocytów, gdzie ulegają podziałom, w wyniku których powstają schizonty wątrobowe. W schizontach następują wielokrotne podziały jąder, tworzą się tysiące merozoitów. Po 6-16 dniach dojrzałe schizonty pękają uwalniając do krwiobiegu merozoity, które wnikają do erytrocytów. W przypadku zarażenia P. vivax i P. ovale większość merozoitów jest uwalniana do krwi, ale część wnika do kolejnych hepatocytów tworząc hipnozoity, których uaktywnienie i przejście w dalszej części cyklu rozwojowego w schizonty krwinkowe może nastąpić w okresie od kilku tygodni do kilku lat, powodując nawrót choroby odległy w czasie. W zarażeniach P. falciparum i P. malariae cykl schizogonii wątrobowej zachodzi jednorazowo. Merozoity dostając się do krwiobiegu i atakując erytrocyty rozpoczynają kolejny etap w cyklu rozwojowym Plasmodium – schizogonię krwinkową. W początkowym okresie rozwoju krwinkowego (do 12 godzin) z merozoitów w erytrocytach powstają trofozoity w postaci tzw. pierścieni. Zarażone krwinki ulegają deformacji. Następnie dochodzi do powstania kolejnej postaci rozwojowej pasożyta – schizontów krwinkowych, które dojrzewając zajmują niemal cała krwinkę czerwoną.
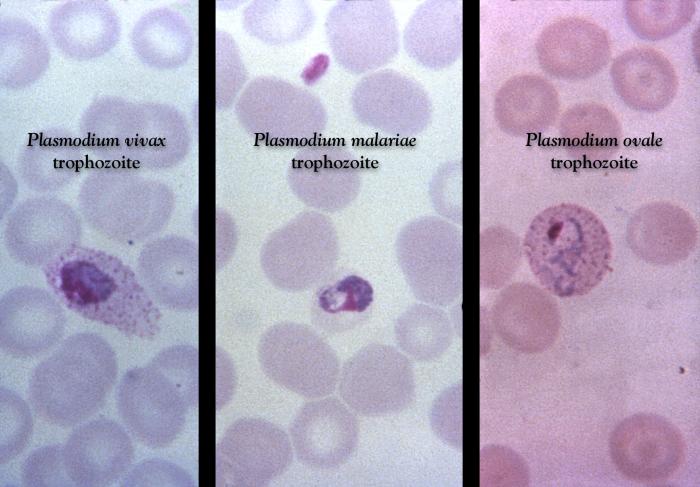
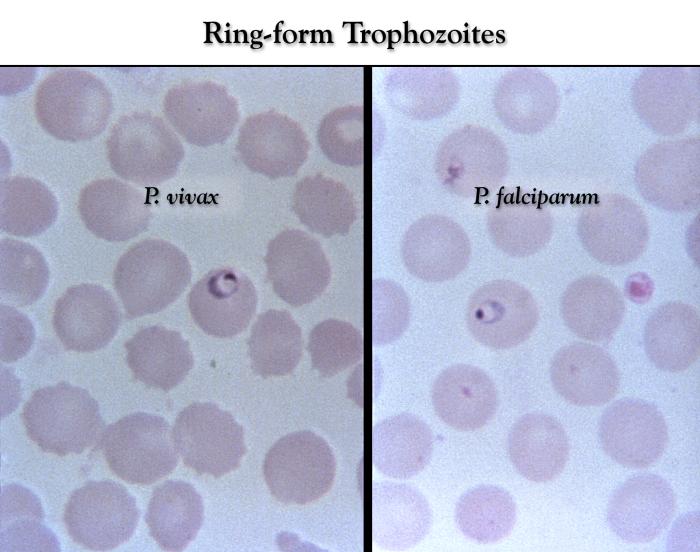
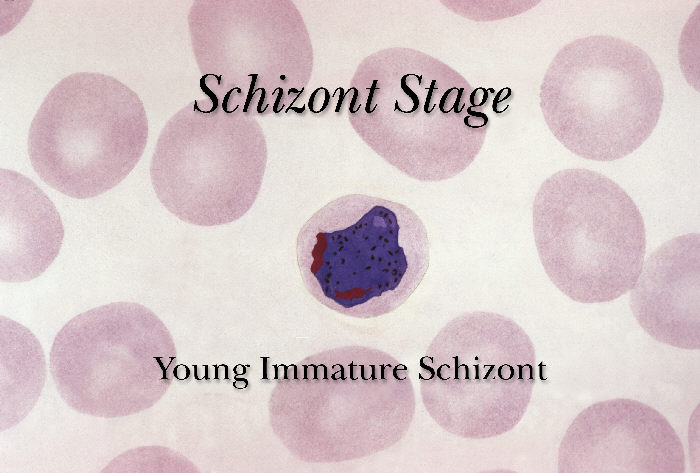
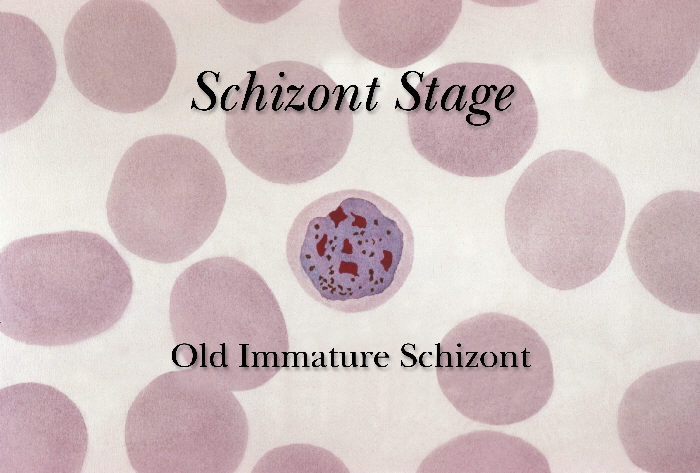
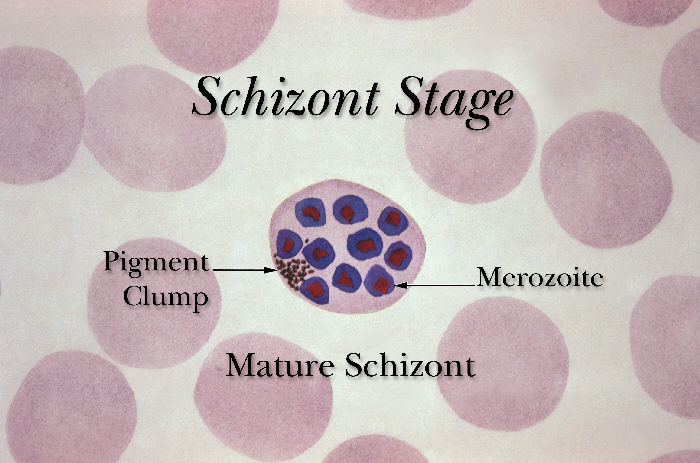
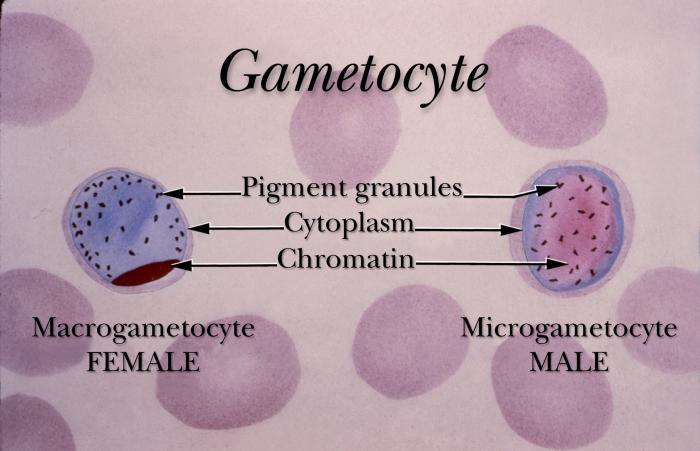
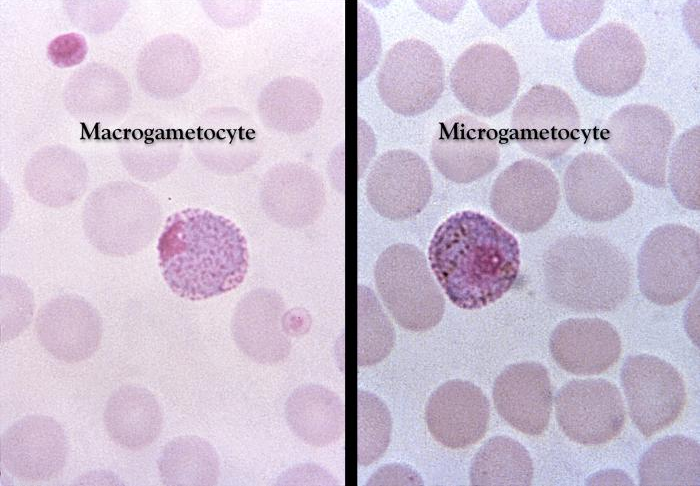
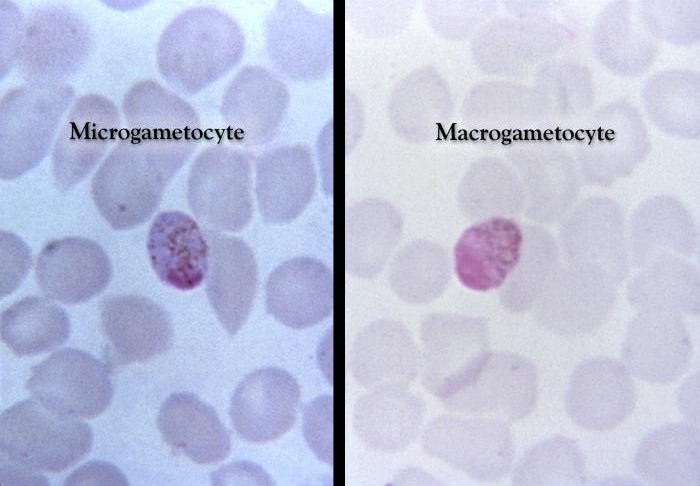
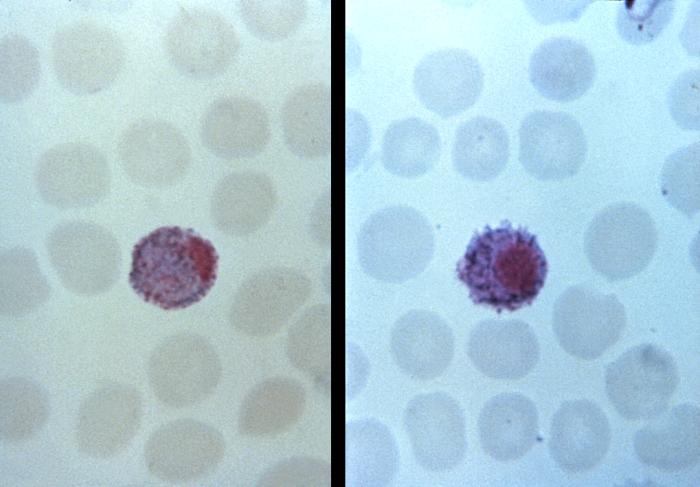
Dojrzałe schizonty pękają uwalniając merozoity (od 6 do 36 w zależności od gatunku), które atakując następne erytrocyty rozpoczynają kolejny cykl schizogonii krwinkowej (pełny cykl trwa zazwyczaj 36-48 godzin w przypadku P. falciparum, 48 godzin – P. vivax i P. ovale oraz 72 godziny – P. malariae). Po kilku-kilkunastu cyklach krwinkowych z części merozoitów rozwijają się postacie płciowe, gametocyty męskie (mikrogametocyty) i gametocyty żeńskie (makrogametocyty), które po wessaniu z krwią przez aparat kłująco-ssący komara rozpoczynają w jego organizmie sporogonię, czyli część płciową cyklu rozwojowego.
Obraz kliniczny Po okresie wylęgania choroby, który jest równy okresowi schizogonii pozakrwinkowej (wątrobowej) i jednemu cyklowi schizogonii krwinkowej (w zależności od gatunku Plasmodium wynoszącemu 9-40 dni), dochodzi do wystąpienia objawów pojawiających się w charakterystycznych, kolejnych trzech fazach: faza zimna (uczucie zimna, dreszcze), faza gorąca (napad gorączki powyżej 40°C, suchość skóry i błon śluzowych, zaburzenia świadomości, śpiączka, bóle brzucha związane z powiększeniem śledziony), faza ustępowania objawów (gwałtowny spadek temperatury ciała ze zlewnymi potami). W przypadku zarażenia Plasmodium vivax i P. ovale *napady gorączki występują cyklicznie co 48 godzin (trzeciaczka), *P. malariae – co 72 godziny (czwartaczka). W zarażeniu P. falciparum napady gorączki są nieregularne, czasami gorączka może ze zmiennym nasileniem utrzymywać się przez cały okres objawowy. Napadom gorączki mogą towarzyszyć bóle mięśni, bóle głowy, nudności, wymioty, biegunka, żółtaczka, powiększenie wątroby i śledziony. Podczas kolejnych napadów gorączkowych dochodzi do powolnego zmniejszania nasilenia objawów, i w przypadku braku powikłań do ich ustąpienia po kilku tygodniach trwania choroby. Malaria wywoływana przez P. falciparum,zwana również malarią złośliwą, charakteryzuje się występowaniem ciężkich powikłań, z wysoką śmiertelnością sięgającą 15-20%. Do objawów stanowiących zagrożenie dla życia pacjenta należą: śpiączka, ogniskowe uszkodzenie ośrodkowego układu nerwowego (malaria mózgowa), ciężka niedokrwistość, skaza krwotoczna małopłytkowa i/lub zespół wykrzepiania wewnątrznaczyniowego, ostra niewydolność krążeniowo-oddechowa, ostra niewydolność nerek, wstrząs, kwasica. Charakterystyczny tor gorączkowy w malarii jest związany z masywnym rozpadem zarażonych erytrocytów oraz ze zmianą struktury i antygenowości zarażonych krwinek czerwonych, w wyniku czego dochodzi m.in. do zespołu hipersplenizmu (oprócz zarażonych erytrocytów, następuje również niszczenie zdrowych krwinek czerwonych, a także płytek krwi). Zarażone i niezarażone elementy morfotyczne krwi tworzą konglomeraty zamykające naczynia włosowate, co prowadzi do niedotlenienia i rozwinięcia zespołu niewydolności wielonarządowej.
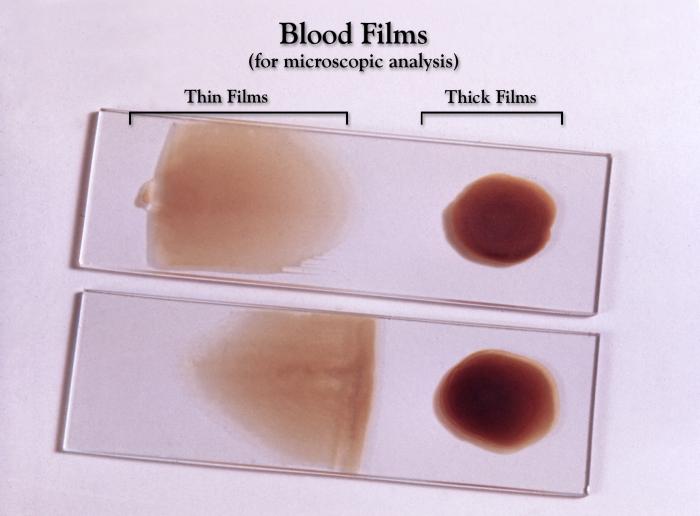
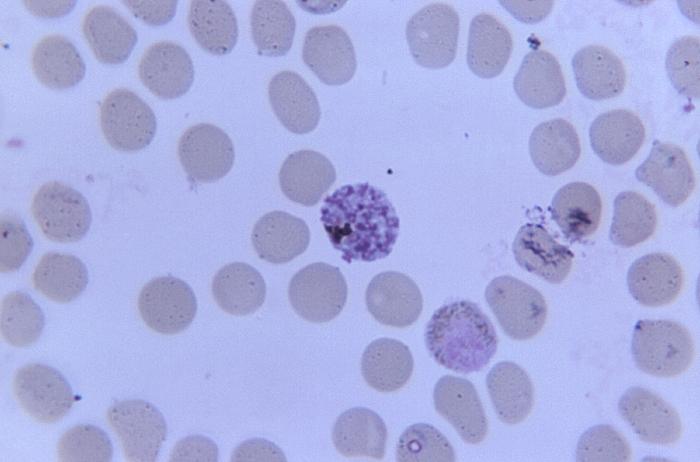
Rozpoznanie Opiera się na stwierdzeniu obecności Plasmodium w preparacie krwi wykonanym metodą grubej kropli (barwienie odczynnikiem Giemzy). Oznaczanie gatunku zarodźca malarii dokonuje się w preparacie krwi wykonanym metodą cienkiego rozmazu (utrwalenie metanolem, barwienie odczynnikiem Giemzy).
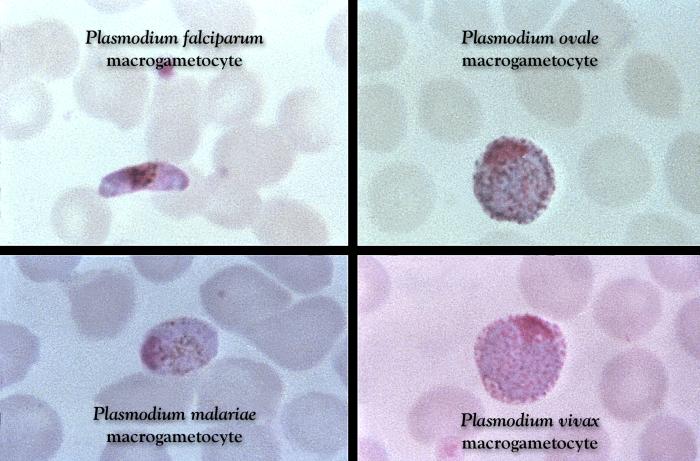
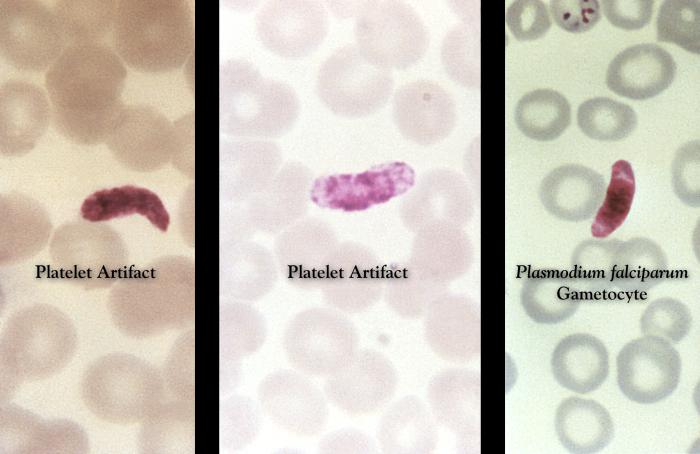
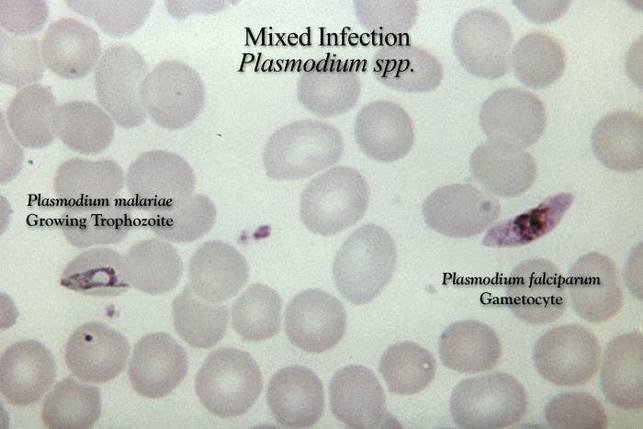
Różnicowanie gatunków Plasmodium z krwi obwodowej w mikroskopii świetlnej opiera się na różnicach w budowie i ilości postaci wewnątrzkrwinkowych w erytrocytach, a także na zmianach kształtu zarażonych krwinek czerwonych. Badania powinny być wykonywane przez doświadczonych diagnostów, wielokrotnie w ciągu kilku dni (w odstępach 6-12-godzinnych). Jednorazowy wynik ujemny nie przesądza o braku zarażenia.
Cechy charakterystyczne poszczególnych gatunków Plasmodium
| P. falciparum | P. vivax | P. ovale | * P. malariae* | |
|---|---|---|---|---|
| okres wylęgania choroby (dni) | 12 (9-14) | 13 (12-17) | 17 (16-18) | 28 (18-40) |
| schizogonia pozakrwinkowa (dni) | 6-7 | 6-8 | 9 | 12-16 |
| liczba merozoitów w jednym hepatocycie | 40000 | 10000 | 15000 | 2000 |
| cykl schizogonii wewnątrzkrwinkowej (godziny) | 36-48 | 48 | 48 | 72 |
| zajęte erytrocyty | wszystkie (głównie młode) | retikulocyty | retikulocyty | starsze krwinki |
| częstotliwość napadów gorączki (godziny) | nieregularnie | trzeciaczka (co 48 h) | trzeciaczka (co 48 h) | czwartaczka (co 72 h) |
| czas trwania napadu gorączki (godz.) | 16-36 lub dłużej | 8-12 | 8-12 | 8 |
| przebieg choroby | ciężki u osób spoza rejonów endemii | średni/ciężki | średni | średni |
| nawroty choroby (obecność hipnozoitów) | nie | tak | tak | nie |
W badaniach przesiewowych coraz częściej wykorzystywane są szybkie testy immunochromatograficzne opierające się na wykrywaniu antygenów Plasmodium. Niska czułość testów powoduje jednak, że wynik negatywny nie wyklucza możliwości zarażenia malarią. W przypadkach wątpliwych metodą diagnostyczną z wyboru, decydującą o rozpoznaniu, jest PCR. W pozostałych badaniach laboratoryjnych oprócz parazytemii (w postaci wywołanej przez P. falciparum zarażonych jest powyżej 2% erytrocytów) dominuje niedokrwistość, trombocytopenia i hiperbilirubinemia.
Leczenie Pacjenci pochodzący z regionów świata, w których malaria nie występuje, a którzy zarazili się w rejonie endemicznego występowania choroby, powinni w każdym przypadku być leczeni jak na ciężką postać choroby (bez względu na jej przebieg kliniczny), gdyż w odróżnieniu od ludności zamieszkującej rejony malaryczne, ich układ odpornościowy może nie być przygotowany na taką odpowiedź immunologiczną w walce z chorobą, jak ma to miejsce u mieszkańców Afryki, Azji czy Ameryki Południowej, którzy zachorowania na malarię często przechodzą wielokrotnie. Jeśli pacjent przyjmował chemioprofilaktykę przeciwmalaryczną i mimo to doszło do zarażenia, w leczeniu choroby należy zastosować inny lek od tego, który był przyjmowany profilaktycznie. Jeśli jednym z objawów choroby są wymioty, które wystąpiły w okresie krótszym niż 30 minut od przyjęcia leku przeciwmalarycznego, dawkę leku należy powtórzyć; jeśli wymioty nastąpiły w okresie 30-60 minut od przyjęcia leku – należy powtórzyć połowę dawki. W przypadku prawdopodobieństwa wystąpienia wymiotów, przed zaordynowaniem leczenia doustnego zalecane jest przyjęcie leku przeciwwymiotnego. W niepowikłanych przypadkach malarii u podróżnych spoza rejonów endemicznych, którzy zachorowali na malarię stosuje się następujące kombinacje leków:
- artemether/lumefantrine
- dihydroartemisinin/piperaquine
- artesunate/amodiaquine
- artesunate/sulfadoxine-pyrimethamine
- artesunate + meflochina
- artesunate + doksycyklina lub klinadamycyna
- atovaquone/proguanil
- chinina + doksycyklina lub klindamycyna
- chlorochina + prymachina
Leczenie opiera się głównie na kombinacji artemizyny lub jej pochodnych (arthemeter, dihydroartemisinin i artesunate) ze środkami farmaceutycznymi należącymi do innych grup leków (ACT, Artemisinin-based combination therapy).
Środki farmaceutyczne stosowane w leczeniu malarii
| Nazwa leku | Dawkowanie |
|---|---|
| artemether/lumefantrine | 6 dawek w ciągu 3 dni: 0, 8, 24, 36, 48, 60 (godz.) 5-14 kg mc: 1 tabl./ jedna dawka 15-24 kg mc: 2 tabl./ jedna dawka 25-34 kg mc: 3 tabl./ jedna dawka >34 kg mc: 4 tabl./ jedna dawka (1 tabl. 20 mg/120 mg) |
| dihydroartemisinin/piperaquine | 4 mg/kg mc dihydroartemisinin + 18 mg km/mc piperaquine 1x dz. przez 3 dni (1 tabl. 40 mg/320 mg) |
| artesunate/amodiaquine | 4 mg/kg mc artesunate + 10 mg/kg mc amodiaquine 1x dz. przez 3 dni (1 tabl. 25 mg/67,5 mg, 50 mg/135 mg lub 100 mg/270 mg) |
| artesunate/sulfadoxine-pyrimethamine | 4 mg/kg mc artesunate 1x dz. przez 3 dni (tabl. 25 mg, 50 mg lub 100 mg) 25 mg/kg mc sulfadoxine (tabl. 500 mg) + 1,25 mg/kg mc pyrimethamine (tabl. 25 mg) jednorazowo w pierwszym dniu leczenia |
| artesunate + meflochina | 4 mg/kg mc artesunate + 8,3 mg/kg mc meflochina 1x dz. przez 3 dni (tabl. 50 mg/250 mg lub 200 mg/250 mg) |
| atovaquone/proguanil | 1 dawka dziennie w ciągu 3 kolejnych dni 5-8 kg mc: 2 tabl. pediatryczne 1x dz. (2x 62,5 mg/25 mg) 9-10 kg mc: 3 tabl. pediatryczne 1x dz. 11-20 kg mc: 1 tabl. dla dorosłych 1x dz. (1x 250mg/100mg) 21-30 kg mc: 2 tabl. dla dorosłych 1x dz. 31-40 kg mc: 3 tabl. dla dorosłych 1x dz. >40 kg mc: 4 tabl. dla dorosłych 1x dz. |
| artesunate + doksycyklina lub klindamycyna | 2 mg/kg mc artesunate + 3,5 mg/kg mc doksycyklina 1x dz. przez 7 dni lub 2 mg/kg mc artesunate 1x dz. przez 7 dni + 10 mg/kg mc klindamycyna 2x dz. przez 7 dni |
| chinina | 8 mg/kg mc co 8 godz. przez 7 dni |
| doksycyklina | dorośli >50 kg: 800 mg przez 7 dni (1 dzień: 2 tabl. w odstępie 12 godz.; 2-7 dzień: 1x1 tabl.) dzieci >8 rż: (leczenie przez 7 dni) 25-35 kg: 0.5 tabl. dziennie 36-50 kg: 0.75 tabl. dziennie >50 kg: 1 tabl. dziennie |
| klindamycyna | <60 kg mc: 5 mg/kg mc 4x dz. przez 7 dni >60 kg mc: 300 mg mc 4x dz. przez 7 dni |
| meflochina | 25 mg/kg mc w dwóch dawkach podzielonych (15 mg/kg mc + 10 mg/kg mc w odstępie 6-24 godz.) |
| chlorochina | 25 mg/kg mc podzielona na trzy dawki dzienne (10 mg/kg, 10 mg/kg i 5 mg/kg) przez 3 kolejne dni (nie stosujemy w zarażeniach wywołanych przez P. falciparum) |
| prymachina | 0,25 mg/kg mc 1x dz. przez 14 dni w Azji Południowo-Wschodniej i na wyspach Oceanii dawkę zwiększyć do 0,5 mg/kg mc (leczenie w zarażeniach wywołanych przez P. vivax i P. ovale) |
W leczeniu malarii wywołanej przez Plasmodium vivax stosuje się jeden z następujących rodzajów farmakoterapii: - chlorochina w połączeniu z prymachiną jest leczeniem z wyboru, jeśli nie stwierdza się oporności na chlorochinę, - dihydroartemisinin/piperaquine lub artemether/lumefantrine w połączeniu z prymachiną stosuje się w przypadkach zarażeń P. vivax opornych na leczenie chlorochiną; jeśli nie ma możliwości zastosowania ww. leków, można zastosować chininę, - aby zastosować u pacjentów prymachinę (niszczy schizonty wątrobowe zapobiegając nawrotom choroby), należy uprzednio wykonać badania w kierunku niedoboru glukozo-6-dehydrogenazy (G6PD), przy którym podczas stosowania leku może dojść do stanów zagrożenia życia z powodu działań niepożądanych, np. hemolizy krwi.
Zarażenia wywołane przez P. ovale mogą być leczone podobnie jak w przypadku zarażenia P. vivax (chlorochina + prymachina). Zarażenia wywołane przez P. malariae mogą być leczone podobnie jak w przypadku zarażenia P. vivax chlorochiną, jednak nie wymagają stosowania prymachiny. Zarażenia wywołane przez P. knowlesi (formy dojrzałe mylone w mikroskopii świetlnej z P. malariae) mogą być leczone podobnie jak niepowikłane przypadki malarii spowodowanej przez inne gatunki Plasmodium.
Leczenie zarażeń wywołanych przez P. falciparum jest bardziej złożone od zarażeń innymi gatunkami Plasmodium, co jest związane przede wszystkim z rosnącą opornością P. falciparum na działanie wielu leków przeciwmalarycznych. Podróżni wracający z podróży z ciężką postacią malarii spowodowanej przez P. falciparum powinni być od początku leczeni na oddziale intensywnej opieki medycznej. Lekiem pierwszego rzutu powinien być wówczas artesunate podawany dożylnie lub domięśniowo, bądź artemether lub chinina w przypadku, gdy artesunate nie jest dostępny. Po pozajelitowym podaniu ww. leków przez okres minimum 24 godzin, należy kontynuować doustną terapię ACT, artesunate + klindamycynę, bądź chininę + klindamycynę.
Środki farmaceutyczne stosowane w leczeniu ciężkich postaci malarii
| Nazwa leku | Dawkowanie |
|---|---|
| artesunate | 2,4 mg/kg mc dożylnie lub domięśniowo 0 h (1 dawka), 12 h (2 dawka), 24 h (3 dawka), następnie 1x dz. dzieci: dawkowanie jak wyżej |
| artemether | 3,2 mg/kg mc domięśniowo (dawka początkowa) kolejne dni: 1,6 mg/kg mc 1x dz. dzieci: dawkowanie jak wyżej |
| chinina | 20 mg/kg mc dożylnie we wlewie lub domięśniowo w 3 dawkach podzielonych co 8 h (dawka początkowa) kolejne dni: 10 mg/kg mc domięśniowo w 3 dawkach podzielonych co 8 h dzieci: dawkowanie jak wyżej uwaga: podawanie dożylne nie może przekroczyć 5 mg/kg mc na godzinę |
Stand-by emergency treatment (SBET, terapia kieszeniowa) W sytuacji, kiedy podróżni znajdują się w rejonach endemicznych malarii, gdzie wystąpiła u nich gorączka niewiadomego pochodzenia, mogąca sugerować zachorowanie na zimnicę, i nie ma możliwości wykonania badań laboratoryjnych potwierdzających lub wykluczających rozpoznanie choroby, należy zastosować we własnym zakresie tzw. terapię kieszeniową (ang. stand-by emergency treatment, SBET) według powszechnie przyjętego dawkowania określonych leków. SBET jest często proponowane pracownikom, którzy przyjeżdżają w rejony malaryczne na zagraniczne kontrakty trwające kilka-kilkanaście tygodni (w Szwajcarii i Wielkiej Brytanii artemether/lumefantrine został zarejestrowany jako lek w terapii SBET dla podróżnych).
Zapobieganie Rodzaj profilaktyki przeciwmalarycznej w zależności od stopnia zagrożenia
| Stopień zagrożenia | Ryzyko transmisji malarii | Zalecana profilaktyka |
|---|---|---|
| I stopień | ograniczone ryzyko transmisji choroby | repelenty, moskitiera |
| II stopień | wyłącznie ryzyko transmisji P. vivax; P. falciparum wrażliwe na chlorochinę | repelenty, moskitiera, chloronina |
| III stopień | ryzyko transmisji P. vivax i P. falciparum; oporność na chlorochinę (Nepal, Sri Lanka, Tadżykistan, niektóre rejony Kolumbii i Indii) | epelenty, moskitiera, chlorochina + proguanil lub atovaquone/proguanil, doksycyklina, meflochina |
| IV stopień | wysokie ryzyko transmisji P. falciparum + wysoka oporność na leki p/malaryczne; umiarkowane/niskie ryzyko transmisji P. falciparum + wysoka oporność na leki; w rejonach o niskim ryzyku transmisji P. falciparum można rozważyć stosowanie repelentów + terapię SBET | repelenty, moskitiera, atovaquone/proguanil, doksycyklina, meflochina (wybór leku w zależności od oporności Plasmodium) |
Środki farmaceutyczne stosowane w chemioprofilaktyce malarii
| Nazwa leku | Dawkowanie | Długość trwania chemioprofilaktyki | Uwagi |
|---|---|---|---|
| atovaquone/proguanil | 1x dziennie 11-20 kg mc: 62,5 mg/25mg (tabletka pediatryczna) 21-30 = kg mc: 2 tabl. pediatryczne 31-40 kg mc: 3 tabl. pediatryczne >40 kg mc: 250 mg/100 mg (tabletka dla dorosłych) 1x1 tabl. | 1 dzień przed wyjazdem, codziennie w trakcie pobytu, 7 dni po powrocie | W 2012 r. lek został zarejestrowany w Polsce do stosowania w chemioprofilaktyce bez ograniczeń czasowych (powyżej 4 tygodni) obniżenie stężenia leku w osoczu przy jednoczasowym przyjmowaniu metoklopramidu lub tetracyklin sporadycznie gastroenterologiczne i dermatologiczne działania niepożądane |
| doksycyklina | 1x dziennie dorośli: 1 tabl. 100 mg | 1 dzień przed wyjazdem, codziennie w trakcie pobytu, 28 dni po powrocie | gastroenterologiczne, ginekologiczne, dermatologiczne działania niepożądane |
| meflochina | 1x tygodniowo dorośli: 1 tabl. 250 mg | 1 tydzień przed wyjazdem, 1x tyg. w trakcie pobytu, 4 tyg. po powrocie | podwyższenie stężenia leku w osoczu przy jednoczasowym przyjmowaniu ampicyliny, tetracyklin lub metoklopramidu neuropsychiatryczne działania niepożądane |
| chlorochina | 1x tygodniowo dorośli: 300 mg (2 tabl. 150 mg) | 1 tydzień przed wyjazdem, 1x tyg. w trakcie pobytu, 4 tyg. po powrocie | przeciwwskazania: epilepsja, łuszczyca |
| chlorochina/proguanil | 1x dziennie >50 kg mc: 100 mg/200 mg (1 tabl.) | 1 dzień przed wyjazdem, codziennie w trakcie pobytu, 28 dni po powrocie | przeciwwskazania: epilepsja, łuszczyca |
| proguanil | 1x dziennie dorośli: 2 tabl. 100 mg | 1 dzień przed wyjazdem, codziennie w trakcie pobytu, 28 dni po powrocie | stosować tylko w połączeniu z chlorochiną |
